Pesquisadores do Caltech e da Universidade do Sul da Califórnia criaram robôs de bolha biocompatíveis que se movem usando reações químicas do corpo, conseguem chegar até regiões tumorais e soltam a carga terapêutica sob comando.
Pesquisadores da Universidade do Sul da Califórnia criam microrrobôs farejadores com enzimas que dentro do corpo humano parecem coisa de filme, mas tem um problema, a maioria das ideias é bonita no slide e chata na vida real. Ou é complexa demais, ou custa caro para fabricar, ou fica difícil de controlar quando entra no tecido vivo, onde tudo é viscoso, apertado e imprevisível.
A sacada deste novo trabalho foi tirar o excesso de engenharia do caminho e apostar no mínimo que funciona: uma bolha.
Sim, uma microbolha, dessas que já são usadas há anos em exames de imagem. A equipe pegou esse “objeto comum” da medicina e transformou em um microrrobô com funções bem diretas: carregar um medicamento, se deslocar até o tumor e liberar a carga no momento certo.
-
Por mais de 400 anos, marinheiros relataram cruzar um oceano que brilhava no escuro como neve, sem ondas e sem reflexos, apenas um brilho uniforme se estendendo até o horizonte, e em 2019 um satélite registrou o fenômeno cobrindo mais de 100.000 km² por mais de 40 noites seguidas ao sul de Java, mas os cientistas ainda não sabem exatamente o que desencadeia o processo

-
Japão vira referência com processo genial que recicla 100 toneladas de plástico por dia usando técnica que remove contaminantes, sensores ópticos que separam PP e PE em segundos e linhas industriais que transformam toneladas de resíduos em paletes reutilizáveis.

-
China criou máquina ‘impossível’ que muda a agricultura ao combinar drones, tratores autônomos com navegação centimétrica, sensores e inteligência artificial

-
A cidade flutuante movida a 2 reatores nucleares que abandona o vapor, usa campos eletromagnéticos para lançar aeronaves ao céu e inaugura uma nova era dos porta-aviões de guerra

O resultado chama atenção justamente por não depender de uma estrutura cheia de peças. Ao invés de impressão 3D, hidrogel e fabricação em sala limpa, o robô nasce como microbolha revestida por proteínas, com ajustes químicos na superfície para acoplar enzimas, fármacos e partículas funcionais. Isso permite produzir muitas unidades parecidas de forma rápida e com custo menor, um ponto que costuma matar projetos de microrrobótica quando tentam sair do laboratório.
Por que uma bolha pode ser um robô e o que ela ganha com isso
A microbolha tem duas vantagens enormes. A primeira é a biocompatibilidade, porque ela já é usada no corpo humano há bastante tempo em aplicações de imagem.
A segunda é que ela é, ao mesmo tempo, cápsula e mecanismo. Ela pode carregar coisas na superfície e também pode ser rompida de maneira controlada, o que vira uma forma limpa de liberação sob demanda.
A equipe criou cápsulas proteicas ao redor das bolhas e, a partir daí, começou a “equipar” essas bolhas como quem coloca funções num canivete.
A química de superfície virou o painel de controle. Dá para acoplar enzima que gera movimento, dá para anexar o medicamento anticâncer e dá para adicionar partículas que facilitam rastreamento ou direção.
O que torna tudo mais interessante é que o sistema permite dois modos de operação. Um mais guiado e outro mais autônomo. E isso conversa com o mundo real, porque nem toda aplicação clínica vai querer o mesmo nível de controle externo.
Como essas microbolhas conseguem se mover sem motor e sem bateria
Aqui entra a parte que faz o leitor arregalar o olho. O movimento não vem de hélice, não vem de bateria, não vem de motor. Ele vem de uma enzima.
Uma das versões usa urease, ligada na superfície da bolha. Essa enzima reage com ureia, um resíduo naturalmente presente no corpo, e gera amônia e dióxido de carbono.
Só que a distribuição da enzima na bolha não é perfeitamente uniforme, então os produtos da reação se acumulam mais de um lado. Isso cria um empurrão químico que impulsiona a bolha para frente.
Na prática, a bolha vira um microrrobô autopropulsionado que se desloca aproveitando o próprio ambiente do corpo. Não é velocidade de Fórmula 1, mas também não precisa ser. A meta aqui é chegar ao lugar certo com eficiência, não correr uma maratona.
Além disso, uma versão inclui nanopartículas magnéticas, o que abre a possibilidade de orientação por ímãs externos, com acompanhamento por ultrassom.
A outra versão busca autonomia de verdade, usando uma segunda enzima para responder a sinais químicos típicos de tumores.
Quando o tumor vira um “cheiro” e o robô segue o gradiente
Tumores e tecidos inflamados tendem a ter concentrações mais altas de certos compostos. Um deles é o peróxido de hidrogênio. Ao adicionar catalase ao sistema, os pesquisadores criaram um mecanismo de resposta a esse gradiente químico.
Traduzindo: o microrrobô passa a “sentir” onde há mais peróxido e a se mover nessa direção, como se estivesse seguindo um rastro.Esse tipo de orientação é conhecido como direcionamento quimiotático.
O detalhe importante é que, nesse modo, o robô não precisa de uma pessoa guiando em tempo real nem de um esquema pesado de controle externo para achar o alvo. Ele usa o ambiente do próprio tumor como bússola.
É aqui que o projeto fica perigosamente interessante, porque ele sugere uma rota de entrega mais precisa com uma estrutura simples. E a simplicidade costuma ser o que permite escala.
Os pesquisadores não ficaram só no discurso de laboratório. Eles testaram o conceito em um modelo animal e colocaram números na mesa, comparando o desempenho da entrega com a terapia convencional.
A descrição completa do método, das duas versões do microrrobô e dos resultados desses experimentos aparece em um estudo publicado na Nature Nanotechnology, que é onde dá para ver com clareza o que foi demonstrado de fato e o que ainda depende de validação em etapas futuras.
O gatilho final é ultrassom e a liberação acontece de uma vez
Chegar no tumor é só metade do problema. A outra metade é fazer o medicamento entrar de verdade no tecido tumoral. Muitos sistemas liberam aos poucos, e isso nem sempre resolve porque a penetração pode ser limitada.
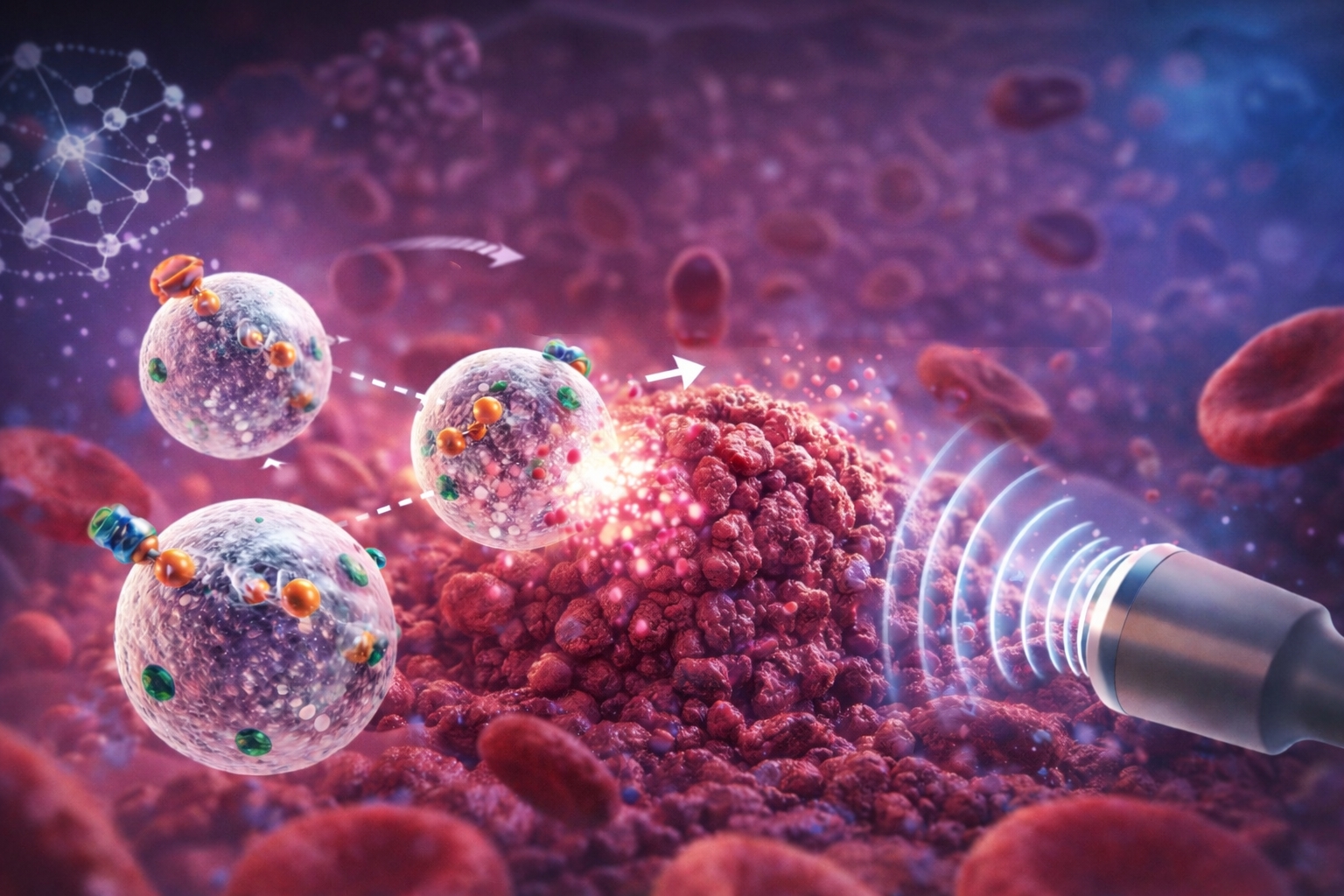
Aqui, a estratégia foi usar ultrassom focalizado para romper a microbolha quando ela atinge o alvo. O colapso é rápido, libera a carga de uma vez e ainda cria um efeito mecânico que ajuda o medicamento a penetrar mais profundamente. É um tipo de entrega que foge do padrão “pingando devagar” e aposta em impacto controlado.
Em experimentos com camundongos com câncer de bexiga, a abordagem levou a uma redução expressiva do peso tumoral ao longo de 21 dias quando comparada a animais tratados apenas com o medicamento, sugerindo que o modo de entrega fez diferença e não só o fármaco em si.
O ponto que faz esse sistema parecer mais pronto para o mundo é a combinação de quatro coisas no mesmo pacote: biocompatibilidade, movimento, capacidade de direcionamento e liberação sob demanda. Tudo isso sem virar um robô caro e impossível de fabricar.








-

Uma pessoa reagiu a isso.